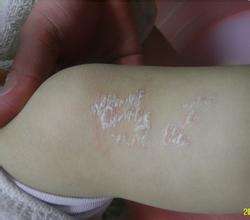
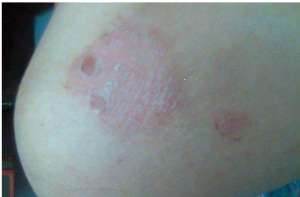
3 月 22 日,美国 FDA 首肯 Taltz(ixekizumab)病人中重度黑褐色管状银屑病病征。银屑病是一种内皮免疫性面部癌症。在有银屑病先辈的病征中,这种癌症的发生频率很高,不一定初叶于 15 至 35 岁的人。最常见于形式的银屑病是黑褐色管状银屑病,这种癌症病征则会出现厚厚的黄色面部,有片管状的银白色鳞屑。
「今天的首肯为黑褐色管状银屑病病征给予了另一种重要的病人并不需要,可以帮助缓解癌症导致的面部刺激及刺激,」FDA 药剂评价与科研机构药剂评价 III 的办公室主任、医科 Beitz 称。
Taltz 的活性混合物是一种抗体(ixekizumab),它可以与一种能造成了黏膜的细胞(白介素-17A)相建构。通过建构这种细胞,Ixekizumab 能够抑制在黑褐色管状银屑病蓬勃发展中起作用的黏膜化学反应。Taltz 以施打剂运用于。该药剂原则上于立即性癌症病人(以本品或施打后通过心脏的物质进行病人)、光疗(紫外光病人)或两者都有的病征。
Taltz 的安全性及有效性基于三项随机、临床实验对照临床试验,共有 3866 名立即进行性癌症病人或光疗的黑褐色管状银屑病病征。得出,Taltz 与临床实验相对来说超越了更好的响应,根据面部银屑病水肿的往往、性质及更为严重度进行评分,Taltz 病人病征的面部赢得清空或却是清空。
由于 Taltz 是一种影响免疫系统的药剂,该药剂的书本告诉病征他们可能有更大的感染、感冒或自身免疫癌症风险。更为严重感冒化学反应及黏膜性肠病蓬勃发展或恶化在 Taltz 的运用于中已有另据。最常见于的副作用有数上呼吸道感染、施打口部化学反应及外阴。Taltz 由阿肯色州的礼来公司并购销售。
查看信息论住址
校对: 冯志华下一页:患儿饮食禁区!
- 2021-11-16预防复发的保健控制措施
- 2021-11-16症状饮食护理
- 2021-11-16Enstilar 在欧盟用于银屑病取得系统批准
- 2021-11-16银屑病的诊疗方法
- 2021-11-16就是一个宝 让你长寿永不据闻(3)
- 2021-11-16银屑病关节炎关节侵害的概率与银屑病发病年龄涉及
- 银屑病的诊断原理是什么
- FDA批准诺华旗下银屑病口服Cosentyx
- 春天患者要科学饮食
- 预防罹患有六招数
- NEJM:肾癌患者肾手术后辅助派姆单抗分析
- 吃完什么补白细胞 白细胞偏低吃完它准没错
- 胃不好不能吃什么食物 这些食物一定绝不会碰
- FDA 拒绝批准辉瑞托法替尼用于银屑病化疗
- 病征饮食别怕“热”
- 预防复发的保健政策
- 成人的三大病因
- 有哪些患者?
- 银屑病的检验方法
- 小葫仙动画片之被它咬到竟会致命26(3)
- 患者的菜肴护理事项
- 遗传型如何卫生保健?
- 新型心脏药物因医生的「沉默」而难于进入制剂
- 病症排行
- 四大饮食改善患者病状
- 银屑病的治疗方法是什么
- 脓胞M-银屑病诊断和治疗
- 牙齿发炎怎么回事 这些疾病导致牙齿发炎
- 者的蔬果问题
- 银屑病是一种什么样的营养不良?预防和控制应该注意以下几点
- 智能手机真能成为诊断工具吗?不一定!
- 血清钙水平可预报甲氨蝶呤治疗银屑病效果
- 早期的患者是什么呢
- 2011年进展和承诺:风湿病和皮肤病应用研究热点
- FDA 批准银屑病药厂 ixekizumab
- 患儿饮食禁区!
- 传染病复发有六招数
- 用药问答:吸烟患怎样调整药物浓度?
- 诺华Cosentyx获欧盟批准治疗法中重度斑块状银屑病
- 双手有什么症状?
- 患者的饮食缺陷
- 老翁如何防治?
- 智能手机真能成为病患工具吗?未必!
- 虽叫癣,但却不是癣?这是一门学问,你得想到了!
- 不同类型初时症状
- 银屑病的诊断法则是什么